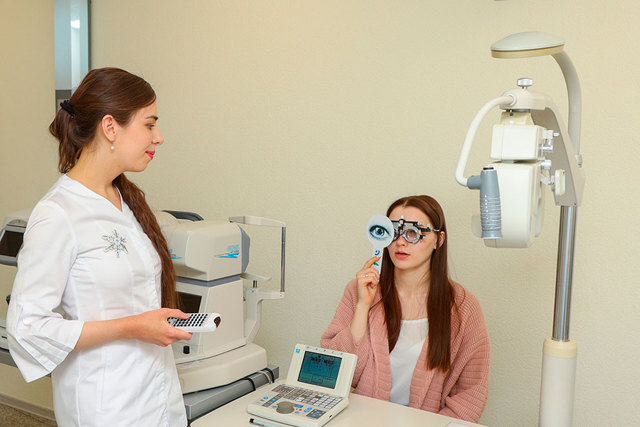
Итак, вы почти решились сделать лазерную коррекцию зрения. Но еще мучают вопросы: каким же будет новое зрение? Как быстро оно войдет в норму и какие есть «подводные камни» в период реабилитации?
Рассказываем!
То, что зрение изменилось, вы почувствуете сразу после завершения операции. Встанете с кушетки и вдруг, например, разглядите циферблат часов в операционной или цифры на настенном календаре. Но вас это может и не впечатлить, так как эмоционально вы все еще там, под прицелом хирургических приборов.
После небольшого отдыха врач еще раз осмотрит ваши глаза, измерит остроту зрения, закапает капли и отпустит вас домой. Врач обязательно расскажет еще и о правилах в реабилитационном периоде, выпишет рецепт и расскажет, что и как правильно капать. Но зачастую пациенты это плохо запоминают, поэтому им дают с собой памятку.
Берите с собой сопровождающего! Пусть он тоже все запоминает. Вам будет непросто читать памятку в первый день после операции.
Начинается этап восстановления после лазерной коррекции зрения.
Первые испытания
И сразу первый «подводный камень»: анестезия перестала действовать и глаза начинают реагировать на произошедшее вмешательство. Лазер испаряет ничтожно малую часть роговицы, но тем не менее это ожог.
Могут появиться болезненность, зуд, чувствительность к свету. Особенно часто такие ощущения появляются после фоторефракционной кератоэктомии.
Организм пытается защитить раневую поверхность, поэтому слезы текут так, что глаз не открыть.
В первое время после коррекции глаз сильно слезится. Так проявляется защитная функция организма
Тут опять выручит сопровождающий. И темные очки! Они не только помогут от слепящего света, но создадут барьер от ветра и пыли на улице. Обязательно возьмите их с собой.
Если некому отвезти вас домой — вызовите такси.
Мы настоятельно не советуем после операции садиться за руль. Это опасно.
Дома свет, по возможности, следует приглушить. Первые несколько часов темнота для глаз комфортнее. Могут наблюдаться звездочки и блики. Это нормально. Скоро они пройдут сами собой. Если болезненность сохраняется и терпеть нельзя, примите таблетку любого обезболивающего.
Главное, ни в коем случае глаза не трогать и не тереть. Даже через закрытое веко. Сильно жмуриться тоже не надо. Слезы аккуратно промакивайте салфеткой под глазами.
Первые сутки после операции очень важно исключить механическое воздействие на глаз. На роговичном лоскуте, который формировали во время лазерной коррекции зрения, могут образоваться складки, или он может сместиться. Это плохо скажется на качестве зрения. Придется опять ехать в клинику и проводить репозицию лоскута.
По этой же причине спать первую ночь рекомендуется на спине. Лучше в очках, чтобы случайно во сне не коснуться глаз.
Новые испытания
Расплывчатое зрение
На утро зрение, скорее всего, будет мутноватым. Не стоит паниковать. В течение часа все наладится. Мозгу нужно время, чтобы привыкнуть к информации, которую теперь передают глаза. От напряженной работы мозга может появиться головная боль.
Синдром сухого глаза
Глаза на следующий день будут сохнуть. Это закономерная реакция организма на слишком обильное слезотечение накануне. Временный синдром сухого глаза развивается у подавляющего большинства пациентов. Сопровождается он зудом и ощущением песка в глазах. Трогать глаза все еще нельзя! Поэтому не умываемся. И не пользуемся косметикой.
Облегчат состояние препараты, которые выписал вам врач. Среди них будут противовоспалительные капли, заменители слезы, а также витаминные комплексы, улучшающие регенерацию тканей.
Проходит синдром сухого глаза у всех по-разному. У кого-то за неделю, кто-то ещё полгода продолжает пользоваться каплями. Это все варианты нормы. Многое зависит от индивидуальных особенностей организма и от того, как сильно вы будете нагружать глаза.
Помогите своим глазам быстрее восстановиться! Глазам нужен покой.
Возьмите больничный, если работа связана с неблагоприятными для глаз факторами. Отложите на время вязание, чтение и просмотр телевизора. Даже от минут 5 серфинга в телефоне сухость глаз заметно усилится.
Скучно? Накачайте заранее себе аудиокниги, слушайте музыку. Прогуляйтесь, но только обязательно в темных очках.
Воспаление
Некоторые пациенты отмечают небольшое покраснение глаз на следующий день после операции. Не надо пугаться. Это не воспаление, а микроразрывы капилляров глаза в ответ на механическое воздействие во время лазерной коррекции. Они пройдут в течение пары дней.
Для профилактики воспаления врач обязательно назначит антибиотики. Капать их нужно строго по схеме, в указанной дозировке. Рана на роговице ещё не зажила и очень уязвима для инфекций.
Есть и положительные моменты
Ваше новое зрение начинает вас радовать! Весь мир, привычные вещи, родственники теперь выглядят иначе, ярче, чётче. Сколько подробностей теперь вы можете разглядеть! Начиная от крупинок на асфальте, и до рисунка на занавесках в окнах соседнего дома.
Будет казаться, что зрение у вас даже больше единицы. Зато вблизи сложновато фокусироваться. Наберитесь терпения. Это этапы стабилизации зрения. Левый и правый глаз, возможно, будут видеть по-разному. Скоро все нормализуется.
Пока зрение стабилизируется, правый и левый глаз могут видеть по-разному. Это нормально.
Не пытайтесь оценивать результаты лазерной коррекции зрения по первым ощущениям!
Зрение будет нестабильным ещё примерно месяц. Но с каждым днем положительная динамика будет все больше и больше.
Испытания продолжаются
Спустя неделю реабилитация после лазерной коррекции зрения идет полным ходом. С утра глаза быстрее «включаются в работу» и видят все лучше и лучше, за компьютером можно провести час или даже два, с перерывами даже дольше. Капли приходится капать реже. Новое зрение становится привычным. Жизнь нормализуется.
Однако полное восстановление глаз после лазерной коррекции зрения еще не произошло. Важно не ослабить дисциплину и продолжить ответственно соблюдать необходимые правила:
- лекарства по расписанию;
- темные очки для выхода на улицу;
- никаких бассейнов, саун и бань;
- спорт пока тоже под запретом.
Физическая активность и высокие температуры, пусть и временно, перегружают организм, и это сразу скажется на качестве зрения. Если ваша работа связана с подъемом тяжестей, лучше взять отпуск.
Но глазам теперь нужен не только покой. Простые упражнения после коррекции зрения помогут им быстрее адаптироваться к новым оптическим характеристикам.
Полезная нагрузка на глаза
Начиная со второй недели после операции, можно выполнять простые, но эффективные упражнения для тренировки глазных мышц, отвечающих за зрение вблизи и вдаль.
Для этого надо попеременно фокусировать взгляд на предметах, расположенных на разных расстояниях. Несколько раз по 3–4 подхода с перерывами. Ничего сложного — минута-две вашего времени, но желательно их делать периодически в течение дня.
За компьютером чаще отвлекайтесь и смотрите в окно.
Если чувствуете напряжение в глазах, сделайте пальминг. Накройте сложенными лодочкой ладонями глаза и немного так посидите. Тепло рук и темнота снимут усталость и улучшат цветовосприятие.
Какой-то особенной гимнастики для восстановления после лазерной коррекции зрения в большинстве случаев не требуется. Зрение постепенно само нормализуется.
Если возникнет необходимость с помощью специальных упражнений поддержать или сохранить качество зрения, врач назначит их после окончательного завершения курса реабилитации. Не раньше чем через месяц после операции.
Поэтому не пренебрегайте контрольными визитами к офтальмологу после операции.
Завершение испытаний
В среднем через месяц после лазерной коррекции зрения основной этап восстановления завершается. Можно оценить результаты.
Вечернее и ночное зрение все еще может быть не идеальными, поскольку восстанавливается дольше — от 3 месяцев до полугода. Но если не увлекаться ночным вождением, то особого дискомфорта это не доставит.
Большинство пациентов возвращается к привычному образу жизни и пользуется новым зрением с удовольствием. О пережитых испытаниях они вспоминают легко и не жалеют о том, что решились на операцию.
Если через месяц зрение начинает ухудшаться, обязательно обратитесь к врачу. Возможно, проблема связана не с корректировкой рефракции, а с другими заболеваниями, которые не были явно выражены на этапе подготовки к операции. Необходимо провести дообследование и назначить лечение.
Чтобы не было разочарований, отнеситесь к выбору клиники ответственно. Перед лазерной коррекцией обязательно проводится комплексная диагностика, обследуется состояние всех отделов глаза, чтобы исключить риск ухудшения зрения.
Полная предоперационная диагностика и качественная работа хирурга — залог хорошего результата лазерной коррекции зрения. Но многое зависит и от самих пациентов, от того, насколько тщательно они соблюдают предписания врача во время реабилитации.
Можно ли восстановить сетчатку глаза — методы восстановления
Всем хочется не только быть по возможности здоровым, но и в случае необходимости получить правильное лечение. К примеру, врачебные манипуляции с глазами, кажутся пациентам необыкновенно страшными из-за особой важности этого органа в жизни человека. Поэтому толика знаний в этом вопросе, никому не будет лишней. В этой статье речь пойдет о сетчатке. Это тончайшая ткань – внутренняя оболочка глаза и периферический отдел зрительного анализатора. Возникающие с ней проблемы всегда очень серьезны и способны поставить под угрозу не только хорошее зрение, но и способность видеть вообще.
Проблемы
Разрушение сетчатки никогда не происходит само по себе. Чтобы это случилось, обязательно воздействие на нее определенных неблагоприятных факторов, которые можно условно разделить на несколько видов:
- Механические воздействия. Это одна из самых распространенных причин повреждения сетчатки. В результате сильной контузии (удара), давления, проникновения внутрь глаза инородного предмета с острыми краями может произойти ее надрыв. Подобные травмы считаются весьма серьезными и требуют оперативного реагирования и длительного восстановления в дальнейшем.
- Заболевания. К истончению, разрывам или отслойке сетчатки могут приводить инфекционные, эндокринные, а также генетические заболевания. При этом, в некоторых случаях подобных заболеваний требуется особый очень деликатный подход к устранению патологии, к примеру, при сахарном диабете.
- Врожденные патологии и возрастные изменения. Возрастные изменения касаются всего организма и сетчатки глаза человека — она становиться тоньше. Нередко, это является причиной ухудшения зрения. Для предотвращения подобной ситуации в зрелом возрасте, в молодости необходимо предпринимать меры профилактики. Профилактика врожденных патологий, увы, невозможна, однако в некоторых случаях подобных состояний, сетчатку удается полностью восстановить.
Методы восстановления сетчатки
Наиболее прогрессивными и действенными сегодня называют сразу несколько методик восстановления сетчатки. Применение их зависит от медицинских показаний, а назначение напрямую связано со сложностью проблемы, причиной повреждения сетчатки и индивидуальными особенностями организма пациента. К подобным методам относят:
- Пептидный. Это способ является уникальным вариантом нехирургического восстановления ткани сетчатки. Воздействие пептидов протекает на клеточном уровне и в результате омолаживает ткани. Пептидами называют вещества, чьи молекулы строятся на остатках α-аминокислот. Главное их свойство – восстановление в клетках процессов метаболизма и синтеза белка. В итоге состояние сетчатки значительно улучшается. Восстановление пептидами или прием пептидов – курс лечения посредством определенных медицинских препаратов. Его обязательно должен назначить специалист, с учетом степени разрушения сетчатой оболочки.
- Лазерный. После операций и проникающих травм, в сетчатой оболочке возможны серьезные нарушения целостности тканей. Для укрепления тканей сетчатки и предотвращения ее отслойки применяют воздействие специальным лазером. Процедура такого воздействия называется лазеркоагуляцией. Кроме лечебного назначения, подобный метод является отличной профилактикой дегенеративных процессов сетчатой оболочки, которые приводят к значительному снижению остроты зрения. Метод имеет свои противопоказания, так применение лазеркоагуляции невозможно в случае некоторых травм глаза. Правда, подобных противопоказаний немного и они всегда озвучиваются лечащим врачом.
- Лечение стволовыми клетками. Фундаментальное изучение свойств стволовых клеток, является приоритетным направлением научной медицины. Ученые многих стран мира посредством стволовых клеток, которые содержатся в пуповинной крови человека, выращивают и регенерируют самые разные его органы и ткани. Сегодня существует возможность получения с помощью стволовых клеток и ткани сетчатой оболочки. Японские ученые наглядно доказали полную безопасен и абсолютную эффективность этого метода. Подобный вариант универсален, его можно применять как после серьезных травм глаза, так и для предотвращения дистрофических процессов сетчатки, возникающих с возрастом. Стволовые клетки помогают полной регенерации клеток сетчатки, а кроме того способствуют выращиванию абсолютно здоровых новых тканей, которые совершенно полноценны и способны активно функционировать. Как правило, регенерация после операции происходит достаточно быстро и процесс реабилитации пациента не занимает много времени. Результаты лечения стволовыми клетками превосходят все самые смелые ожидания, что делает его необыкновенно популярным среди специалистов.
Видео нашего врача по теме
В заключение стоит напомнить, что восстановление сетчатки возможно и для этого существует несколько медицинских способов. Назначение того или иного метода лечения происходит при определенных показаниях. К ним относят: степень разрушения сетчатки, его причины, физические данные пациента. Также необходимо запомнить, что при первых признаках ухудшения зрительных функций, особенно после травмы глаза, необходимо по возможности быстро обратиться к специалисту-офтальмологу. Лишь в этом случае можно говорить о своевременном лечении, которое должно принести хорошие результаты.
Обратившись в Московскую Глазную Клинику, каждый пациент может быть уверен, что за результаты лечения будут ответственны одни из лучших российских специалистов.
Уверенности в правильном выборе, безусловно, прибавит высокая репутация клиники и тысячи благодарных пациентов.
Самое современное оборудование для диагностики и лечения заболеваний глаз и индивидуальный подход к проблемам каждого пациента – гарантия высоких результатов лечения в Московской Глазной Клинике. Мы проводим диагностику и лечение у детей старше 4 лет и взрослых.
{loadposition doc-vitamin}
Уточнить стоимость той или иной процедуры, записаться на прием в «Московскую Глазную Клинику» Вы можете по телефону 8 (800) 777-38-81 (ежедневно с 9:00 до 21:00, бесплатно для мобильных и регионов РФ) или воспользовавшись формой онлайн-записи.
Не надо ехать в Швейцарию: В Петербурге научились сохранять зрение детям со "светящимся глазом"
Когда детский офтальмолог обнаруживал редкое онкологическое заболевание – ретинобластому, он советовал родителям везти ребенка на лечение в Швейцарию.
Теперь это орфанное – редкое заболевание лечат и в Петербурге.
Как любое другое онкологическое заболевание, врожденная онкологическая опухоль глаза лечится тем лучше, чем раньше ее выявят.
Признаки, которые должны насторожить родителей – нистагм, внезапно появившееся косоглазие.
Рђ еще — «светящийся глаз»: если РЅР° фотографии, сделанной СЃ вспышкой, Сѓ ребенка зрачок оказывается РЅРµ красным Рё РЅРµ черным, Р° белым – надо срочно бежать Рє врачу.
С рождения у Алии мама замечала нистагм (непроизвольные движения глаз). Но ни невролога поликлиники, ни офтальмолога это не настораживало.
Тогда мама сама пошла на прием в Педиатрический университет (СПБГПМУ).
Там и выявили изменения на глазном дне, диагноз – «билатеральная ретинобластома», врожденное онкологическое заболевание глаз, проще говоря, злокачественная опухоль.
Оно настолько редкое, что составляет всего 4% от всех онкологических заболеваний у детей. Не каждый врач встречается с ним даже за всю свою профессиональную жизнь.
— После первого РєСѓСЂСЃР° химиотерапии Сѓ Алии появилось косоглазие, после РґРІСѓС… РєСѓСЂСЃРѕРІ результата РЅРµ было, — рассказывает мама девочки.
– Тогда врачи начали проводить селективную химиотерапию. Уже после второго курса дочь начала видеть игрушки, хотя левый глаз пока видит хуже правого.
Алия – обычный 9-месячный ребенок, отставаний в развитии нет. Опухоль уменьшилась с 12 мм до 5-6 мм.
Хочу предупредить всех родителей: очень важно, чтобы осмотры у офтальмолога проводились на расширенном зрачке. �наче врачи ничего не увидят.
Как не увидели, например, у еще одного пациента, которому скоро исполнится 5 лет.
«Он для такого заболевания старичок», — РіРѕРІРѕСЂРёС‚ его мама, потому что РѕРЅРѕ выявляется как правило, РІ самом раннем возрасте.
Его опухоль была обнаружена в поликлинике случайно и ребенка направили в больницу им. Раухфуса.
Куда бы дети не направлялись, ими занимаются специалисты трех петербургских клиник: сейчас весь цикл лечения проводится мультидисциплинарной командой НМ�Ц онкологии им. Н.Н.
Петрова, Детского городского многопрофильного клинического центра высоких медицинских технологий им. К. А.
Раухфуса, Санкт-Петербургского государственного педиатрического медицинского университета.
— Раньше РјС‹ РЅРµ видели таких детей, — РіРѕРІРѕСЂРёС‚ Светлана Кулева, заведующая отделением химиотерапии Рё комбинированного лечения злокачественных опухолей Сѓ детей РќРњР�Р¦ онкологии РёРј. Рќ.Рќ. Петрова. – Потому что детские офтальмологи, увидев такую патологию, терялись Рё рекомендовали отправляться РЅР° лечение РІ швейцарскую клинику.
Хотя, как рассказали сотрудники СПбГПМУ, у них есть пациент, пролеченный еще 23 года назад, но ему один глаз пришлось удалить.
Появлению новых, сохраняющих глаза и зрение методов лечения детских глазных опухолей мы обязаны Японии.
Родители детей отказывались от энуклеации (удаления глаза), предпочитая смерть ребенка от прогрессирования опухоли в силу национальных особенностей.
Р’ 1990 годах СЏРїРѕРЅСЃРєРёРµ С…РёСЂСѓСЂРіРё-офтальмологи изобрели метод интравитреальной химиотерапии (методика РЎР�РђРҐРў) — введение химиопрепарата непосредственно РІ глазничную артерию, что РїСЂРёРІРѕРґРёС‚ Рє гибели опухоли без развития системных осложнений химиотерапии Рё сохранению глаза.
Затем появлялись новые методы лечения: схема химиотерапии CEV (карбоплатин + этопозид + винкристин), ставшая золотым стандартом лечения РІ комбинации СЃ такими физическими методами воздействия, как криодеструкция Рё лазерокоагуляция. Рто позволило свести Рє РјРёРЅРёРјСѓРјСѓ необходимость удаления глаз Рё дистанционной лучевой терапии (ее применение увеличивало СЂРёСЃРє развития вторых опухолей). Сейчас, РєРѕРіРґР° есть возможность устанавливать диагноз РЅР° ранних сроках, Сѓ большинства детей выживаемость РїСЂРё ретинобластоме стремится Рє 100%, Рё самым важным для врачей Рё пациентов стало РЅРµ только сохранение глаза, пораженного опухолью, РЅРѕ Рё избавление ребенка РѕС‚ слепоты.
Р’ Петербурге РІСЃРµ пациенты СЃ подозрением РЅР° ретинобластому направляются офтальмологами первичного звена РІ офтальмологические отделения РіРѕСЂРѕРґР°: РІ многопрофильный центр РёРј. Рљ.Рђ. Раухфуса, СПбГПМУ, Р° жители области — РІ Ленинградскую областную детскую больницу. Здесь проводится дополнительное обследование — офтальмоскопия СЃ фотофиксацией РЅР° ретинальной камере, ультразвуковое исследование глаз. Затем пациент переводится РІ РќРњР�Р¦ онкологии РёРј. Рќ.Рќ. Петрова, РіРґРµ дообследуется, чтобы исключить распространение опухоли – выполняется РњР Рў, РЈР—Р� регионарных лимфатических узлов Рё РґСЂ. РџРѕ результатам комплексного обследования детский онколог составляет программу лечения.
Системная химиотерапия проводится РІ детском отделении центра РёРј. Рќ.Рќ. Петрова. Химиохирургический метод — селективная интраартериальная химиотерапия, РІ клинике СПбГПМУ.
Методы локального контроля — лазерокоагуляция, криотерапия – РІ профильном офтальмологическом отделении СПбГПМУ или Детского клинического центра РёРј. Раухфуса.
РљСЂРѕРјРµ того, РІ этих РґРІСѓС… клиниках успешно проводится лечение СЃ применением методики интравитреальной химиотерапии — введение химиопрепарата РІ стекловидное тело через супертонкую иглу.
Уже в этом году планируется внедрение методики С�АХТ в клинике НМ�Ц онкологии им. Петрова после модернизации отдела интервенционной радиохирургии.
Рто позволит сконцентрировать системные Рё локальные химиотерапевтические методики РІ РѕРґРЅРѕРј центре.
РќРѕ РїРѕРєР° врачам РЅРµ хватает еще РѕРґРЅРѕР№ возможности для эффективного лечения маленьких пациентов — брахитерапии (местной лучевой терапии) СЃ использованием офтальмоаппликаторов СЃ радиоизотопами Ru-106 Рё Sr-90 – РІ Р РѕСЃСЃРёРё нет препаратов, рассчитанных РЅР° детей. Рђ РѕРЅР° очень нужна РІ качестве второй линии РїСЂРё неудачах предшествовавшего лечения или первично — РїСЂРё опухолях небольших размеров.
Об этом детские офтальмологи и онкологи говорили на V Петербургском международном онкологическом форуме «Белые ночи», который проходит в эти дни в Петербурге.
Ретинобластома – онкологическое заболевание поражающее глаза у детей раннего возраста. Его можно отнести к редким, так как оно встречается в среднем у одного из 16 – 18 тысяч новорожденных.
Удельный вес ретинобластомы РІ структуре злокачественных опухолей детского возраста РЅРµ велик — РѕС‚ 1,1 РґРѕ 3,8 %.
В структуре глазной заболеваемости опухоль составляет от 0,001 до 0,008%, а детской глазной заболеваемости — 0,07%.
70% выявленных опухолей – ненаследственные (спорадические) Остальные 30% представлены наследственно-обусловленной формой – в таком случае, как правило, поражены оба глаза. Около 95% случаев ретинобластомы диагностируются до 5 лет.
В Северо-Западном регионе ежегодно выявляют не более 20 новых случаев ретинобластомы. Статистика по России неизвестна, так как это заболевание включают в группу онкологических заболеваний глаз.
�сточник
Темпы восстановления остроты зрения после хирургического лечения макулярных разрывов с интраоперационным применением оптической когерентной томографии и различных методов визуализации внутренней пограничной мембраны
В настоящее время положительный результат хирургического лечения макулярных разрывов диаметром до 400 мкм достигается в большинстве случаев [1]. Определенную сложность представляет полное закрытие макулярных разрывов диаметром больше 400 мкм.
- Для решения проблемы предложено множество техник: механическое сближение краев разрыва пинцетом или канюлей с силиконовым кончиком, большой диаметр удаления внутренней пограничной мембраны (ВПМ), инвертированный лоскут ВПМ, тампонада разрыва тромбоцитарной массой, газом, перфторорганическим соединением (ПФОС) и силиконовым маслом [2, 3].
- В хирургическом лечении макулярных разрывов большого диаметра мы применяем специфическую технику анатомической реконструкции фовеолы, суть которой состоит в удалении ВПМ сетчатки без окрашивания, и используем последовательную технику механического сближения краев разрыва в трех средах (жидкости, воздухе и ПФОС) с помощью мягкой силиконовой канюли, когда достигается полное высушивание дна разрыва и производится прямая замена ПФОС на силиконовое масло [4, 5].
- Как известно, одной из наиболее частых причин низких визуальных исходов хирургического лечения макулярных разрывов являются атрофические изменения пигментного эпителия и частичная атрофия диска зрительного нерва, вызванные токсическим действием применяемых для контрастирования ВПМ витальных красителей (особенно бриллиантового зеленого), о чем свидетельствуют данные не только биомикроскопического обследования, но и электроретинографии [6, 7].
Можно согласиться с доминирующим среди витреоретинальных хирургов мнением, что применение красителей существенно упрощает механическое удаление полупрозрачной ВПМ, снижая риск ятрогенного повреждения сетчатки и улучшая анатомический результат. Поэтому поиск наименее токсичных красителей является актуальной проблемой [8].
Наименее токсичными признаны красители BBG и Membrane Peel, которые выпускаются фирмами DORC (Голландия) и Geuder (Германия). Однако и они не лишены токсичных свойств (по стандартам DIN EN ISO 10993), на что указывают сами производители (табл. 1)
Таблица 1. Сведения о цитотоксичности производимых красителей для ВПМ в соответствии с DIN EN ISO 10993 [9].
Сегодня на рынке не существует абсолютно нетоксичных красителей, а их цитотоксический эффект определяется концентрацией того или иного химического агента. Обзор литературы по проблеме использования красителей был представлен в нашей ранней публикации [10].
В результате многолетней практики нам удалось найти 7 способов облегчения визуализации ВПМ в ходе операции (их описание требует отдельной статьи), что позволило уйти от применения красителей в хирургическом лечении макулярных разрывов.
Одним из критериев оценки результатов хирургического лечения макулярных разрывов является восстановление максимально корригированной остроты зрения (МКОЗ). Этот показатель и был взят за основу исследования.
Цель работы — оценить скорость восстановления МКОЗ и анатомические результаты хирургического закрытия больших макулярных разрывов сетчатки у пациентов, оперированных с применением витальных красителей и без них.
Материалом исследования послужили 160 пациентов (190 глаз) со сквозными макулярными разрывами диаметром от 400 до 900 мкм, которые были прооперированы с декабря 2011 по март 2016 г.
Все пациенты в зависимости от метода удаления ВПМ были разделены на 2 группы: основную (130 глаз), в которой ВПМ удаляли без окрашивания, и контрольную (60 глаз), где для окрашивания ВПМ использовали краситель трипановый голубой. Данные пациентов обеих групп представлены в табл. 2.
Таблица 2. Распределение оперированных пациентов (глаз) по группам Примечание. Здесь и в табл.3, 5: СО — среднее отклонение.
Всем пациентам были выполнены визометрия по таблице Сивцева—Головина, оптическая когерентная томография (ОКТ) с помощью томографа третьего поколения Stratus («Carl Zeiss», Германия) и фотоконтроль.
Техника операций. Все операции в обеих группах выполнены с использованием трехпортового доступа к полости стекловидного тела и разового набора инструментов калибра 27G.
В обеих группах для освещения витреальной полости использовали желто-зеленый ртутный свет Photon II, обладающий низкой фототоксичностью [4], с одинаковой яркостью светового потока 1000 люкс (не более 2% от мощности), которая была замерена с помощью отечественного люксометра «ТКА-ПКМ».
Вторым этапом в обеих группах проводили субтотальную витрэктомию с использованием аппарата CONSTELLATION Vision System («Alcon», США), отделение и удаление задней гиалоидной мембраны (ЗГМ) после предварительного контрастирования кеналогом с помощью витреотома ULTRAVIT 25+ и 27+. Следующим этапом выполняли дозированное удаление ВПМ по предложенному нами способу (Авторское свидетельство RU 02409332 «Способ хирургического лечения макулярных разрывов», Байбородов Я.В., Балашевич Л.И., от 20.01.2011) [11].
В основной группе пилинг осуществляли без окрашивания ВПМ с использованием принципов визуализации прозрачных структур.
Для захвата ВПМ без применения красителя использовали витреоретинальный концезахватывающий пинцет № 43 («Alcon Grieshaber AG», Швейцария).
В контрольной группе ВПМ предварительно окрашивали введением в полость глаза красителя трипанового голубого в концентрации в 2 раза ниже предлагаемой производителем — 0,075%.
- Как в контрольной, так и в основной группах применяли специфическую технику полного интраоперационного закрытия разрыва: последовательно сближали края разрыва в трех разных средах: в воде, в воздухе, в ПФОС.
- Окончательное интраоперационное закрытие разрыва производили в среде ПФОС: аспирация жидкости из разрыва приводила к полному сближению его краев, затем для исключения повторного расхождения краев разрыва из-за затекания в него внутриглазной жидкости производили прямую замену ПФОС на силиконовое масло, что позволяло удерживать края разрыва сомкнутыми.
- У части пациентов (30 глаз) основной группы процесс закрытия макулярного разрыва контроливался с помощью оптического когерентного томографа высокого разрешения RESCAN 700, интегрированного в операционный микроскоп OPMI LUMERA 700 («Carl Zeiss Meditec», Германия).
- Силиконовое масло удаляли, как правило, через 1 мес после первой операции.
- Закрытием макулярного разрыва мы считали полное сопоставление его краев с отсутствием анатомического дефекта нейроэпителия.
Края больших макулярных разрывов, сближенные интраоперационно, оставались сомкнутыми и на следующий день после операции, что позволило сократить время положения пациента лицом вниз до 2—3 дней (рис. 1).
Рис. 1. Клиническийслучай 1. ОКТ-снимки (а, б) и фотографии глазного дна (в, г). а — до операции: диаметр разрыва 756 мкм, атрофии ПЭ нет, МКОЗ =0,3; б — на следующее утро после операции с применением техники сближения краев разрыва: разрыв закрыт, атрофии ПЭ нет, МКОЗ =0,7; в — до операции; г — на следующий день после операции.
Острота зрения на следующий день после операции в контрольной и основной группах представлена в табл. 3.
Таблица 3. Анатомические и визуальные показатели на следующий день после операции
Статистическую зависимость остроты зрения от применяемых оперативных техник на следующий день после операции устанавливали с использованием критерия Кохрана—Мантеля—Гензеля (Cohrane—Mantel—Haenzel) (табл. 4).
Таблица 4. Статистическая зависимость остроты зрения от применяемых оперативных техник на следующий день после операции
Сравнительная оценка функциональных и анатомических показателей обеих групп представлена в табл. 5.
Таблица 5. Анатомические и визуальные показатели в период наблюдения 1 год Примечание. ПЭ — пигментный эпителий.
Статистическую зависимость функциональных и анатомических показателей от применяемых оперативных техник через 1 год после операции устанавливали с использованием критерия Кохрана—Мантеля—Гензеля (Cohrane—Mantel—Haenzel) (табл. 6).
Таблица 6. Статистическая зависимость функциональных и анатомических показателей от применяемых оперативных техник через 1 год после операции
Различия считали достоверными при уровне вероятности меньше 0,05. Как следует из табл. 6, все различия в группах являются статистически значимыми. В статистике учитывали также ненулевую корреляцию, общую ассоциацию и среднее отличие между двумя группами.
Обследование пациентов после операции (биомикроофтальмоскопия, фотоконтроль, оптическая когерентная томография (ОКТ)) показало, что атрофия пигментного эпителия чаще встречалась в контрольной группе, в которой проводилось окрашивание ВПМ (рис. 2, 3).
Рис. 2. Клинический случай 2. ОКТ-снимки (а, б) и фотография глазного дна (в). а — до операции: диаметр разрыва 546 мкм, атрофии ПЭ нет; б — после операции с применением трипанового голубого красителя: разрыв закрыт, атрофия ПЭ (инфракрасное излучение ОКТ проходит глубже узкой полоской через ПЭ); в — после операции: атрофия ПЭ в фовеоле. Рис. 3. Клинический случай 3. ОКТ-снимки (а, б) и фотография глазного дна (в). а — после операции: диаметр =580 мкм, атрофии ПЭ нет; б — после операции без применения красителя: разрыв закрыт, высокая оптическая плотность ПЭ в фовеоле; в — визуальных признаков атрофии ПЭ не обнаруживается.
Витрэктомия (190 глаз) провоцировала развитие катаракты у подавляющего большинства пациентов: через 6 мес после хирургии на 160 (84%) глазах развилась катаракта.
В основной группе мы не окрашивали ВПМ и с целью ее визуализации применяли желто-зеленый осветитель. Зеленое излучение осветителя создает эффект, подобный осмотру в бескрасном свете, облегчающем визуализацию ВПМ и слоя нервных волокон.
В обеих группах с целью устранения влияния светового повреждения сетчатки на конечный результат для освещения витреальной полости использовался желто-зеленый ртутный свет от прибора Photon II, обладающий низкой фототоксичностью [4], с очень низкой яркостью светового потока — 1000 люкс (это меньше, чем обычно используют хирурги, как минимум в 3 раза). И сегодня подобная минимальная иллюминация (до 10% мощности) позиционируется за рубежом только в неразрывной связке с применением новой технологи «3D Heads Up» [12].
В применении так называемых «витальных» красителей для удаления ВПМ сегодня уже нет необходимости, поскольку синтез принципов визуализации прозрачных структур и современного уровня техники, включающий в себя зеленый источник света и интраоперационный ОКТ-контроль, способствует точности хирургического действия (рис. 4).
Рис. 4. Удаление ВМП без окрашивания с помощью интраоперационного ОКТ-контроля. а — процесс удаления (на ОКТ-срезе видна тень от пинцета, которая не препятствует визуализации мембраны); б — интраоперационный динамический контроль (на ОКТ- срезе виден остаток ЗГМ и край ВПМ). На рис. 4, б видна неокрашенная ВПМ, которую можно захватить пинцетом.
Следует отметить, что края макулярного разрыва сближались у всех пациентов. Интраоперационный ОКТ-контроль позволял получать обратную связь от сетчатки, показывая наличие жидкости, и обеспечивал точность сближения краев макулярного разрыва после его дренирования.
В отличие от тампонирующих непосредственно макулярный разрыв методик, техника полного интраоперационного сближении краев большого макулярного разрыва в трех средах (жидкости, воздухе и ПФОС) с дренированием жидкости из разрыва в среде ПФОС и последующей прямой его заменой на силиконовое масло приводит к значительному увеличению остроты зрения за короткий срок, видимо, вследствие анатомического восстановления фовеолы и создания оптимальной плотности колбочек в фовеолярной зоне (рис. 5)
Рис. 5. Закрытие макулярного разрыва под интраоперационным ОКТ-контролем. Снимки. а — в начале операции до удаления ВПМ; б — после полного закрытия разрыва. [2—5]. Удаление силикона в сроки до 1 мес позволяет избежать побочных эффектов длительной силиконовой тампонады.
В отличие от описанной нами технологии, методики тампонирования макулярных разрывов большого диаметра (больше 400 мкм) различными дериватами (лоскуты ВПМ, тромбоциты, кровь и т. д.
) без сближения краев макулярного разрыва способствуют их закрытию вследствие образования соединительной ткани в фовеоле.
Применение техники прямой замены ПФОС на силикон после высушивания макулярного разрыва позволяет не использовать для его тампонады фрагменты ВПМ.
Известно, что острота зрения определяется расстоянием между двумя колбочками и, соответственно, чем плотнее нейроэпителий в зоне фовеолы, тем она выше.
1.
Использование щадящей техники (удаление ВПМ сетчатки без окрашивания, с применением желто-зеленого света c низкой фототоксичностью в режиме очень низкой яркости светового потока) имеет выраженное преимущество по сравнению с традиционной техникой (включающей окрашивание ВПМ трипановым голубым красителем), заключающееся в очень быстром восстановлении МКОЗ (в течение одних суток) у пациентов с макулярными разрывами диаметром больше 400 мкм.
2.
Техника анатомической реконструкции фовеолы вследствие полного сближения краев большого макулярного разрыва в трех средах, дренирования жидкости из разрыва в среде ПФОС и удерживания краев сомкнутыми в конце операции при прямой замене ПФОС на силиконовое масло с контролем за процессом при помощи встроенного в микроскоп оптического когерентного томографа приводит к высоким анатомическим и функциональным результатам.
Участие авторов:
Концепция и дизайн исследования: Я.Б.
Сбор и обработка материала: Я.Б., К.Ж., И.Х.
Статистическая обработка: Я.Б., К.Ж., И.Х.
Написание текста: Я.Б.
Редактирование: Я.Б., К.Ж.
- Авторы заявляют об отсутствии конфликта интересов.
- Сведения об авторах
- Жоголев Константин Сергеевич — врач-офтальмолог
- e-mail: ksjogolev@rambler.ru
- orcid.org/0000-0002-4547-4117