Возрастная макулярная дегенерация
Название: Болезнь Штаргардта.
Болезнь Штаргардта
Болезнь Штаргардта. Наследственное заболевание сетчатки, которое проявляется дистрофическими изменениями ее макулярной зоны и приводит к потере центрального зрения. Дебют заболевания приходится на детский или юношеский возраст. У пациентов отмечаются центральные скотомы и нарушения цветового зрения.
Прогрессирование болезни Штаргардта приводит к полной слепоте. Диагностика проводится с помощью офтальмоскопии, флуоресцентной ангиографии и ЭФИ сетчатки.
Для лечения применяется инъекционная терапия (витамины, антиоксиданты, ангиопротекторы), физиотерапия, проводятся реваскуляризирующие операции, разрабатывается методика аутологичной тканевой терапии.
Другое название болезни Штаргардта – ювенильная макулярная дегенерация – отражает суть заболевания: оно начинается в юном (ювенильном) возрасте и характеризуется поражением макулы – рецепторного аппарата зрительного анализатора.
Заболевание описал немецкий офтальмолог Карл Штаргардт в начале ХХ века как врожденное поражение макулярной области глаза, которое передавалось по наследству в одной семье. Типичные офтальмоскопические признаки болезни Штаргардта полиморфны: «атрофия хориоидеи», «бычий глаз», «битая (кованая) бронза».
Патогенетическое название патологии – «желтопятнистая абиотрофия сетчатки» — отражает изменения в области глазного дна. В 1997 году генетики обнаружили мутацию гена АВСR, вызывающую нарушение выработки белка, который должен переносить энергию фоторецепторным клеткам.
Неполноценность переносчика АТФ приводит к гибели фоторецепторов сетчатки глаз. Различные виды наследственно обусловленной макулярной дистрофии встречаются в 50% случаев патологии глаз. Из них болезнь Штаргардта составляет около 7%. Нозологическая форма диагностируется с частотой 1:10000 и характеризуется прогрессирующим течением.
Двусторонняя патология глаз начинается в молодом возрасте (от 6 до 21 года) и приводит к тяжелым последствиям, вплоть до полной потери зрения. Заболевание имеет социальную значимость, потому что приводит к инвалидности в молодом возрасте.
Болезнь Штаргардта Наследование не зависит от половой принадлежности пациента и родителей. Патология передается преимущественно по аутосомно-рецессивному типу, то есть наследование патологии не связано с полом (аутосомное – связано с неполовыми хромосомами) и не всегда передается будущему поколению (рецессивный путь наследования). По последним данным врачей-генетиков, патология гена может передаваться и по доминантному типу. При доминантном типе наследования дефектов гена – контролера синтеза белка-транспортера АТФ – заболевание протекает легче и нечасто приводит к инвалидности. Большинство рецепторных клеток макулы (верхушки) желтого пятна глазного дна функционируют. У пациентов с доминантным типом наследования болезнь протекает с минимумом проявлений. Больные сохраняют работоспособность и могут даже водить автотранспорт. Основная причина дегенерации клеток макулы заключается в том, что они страдают от дефицита энергии. Дефект гена приводит к синтезу неполноценного белка, транспортирующего молекулы АТФ через мембрану клеток желтого пятна – центра сетчатки глаза, в котором фокусируется графическое и цветное изображение. В области желтого пятна нет кровеносных сосудов. Питание клеток-колбочек осуществляется за счет белков-переносчиков АТФ из близлежащей сосудистой оболочки (хориоидеи). Белки переносят через мембрану внутрь клеток-колбочек молекулы АТФ.
В нормальных условиях родопсин фоторецепторов поглощает фотон света, трансформируясь в транс-ретиналь и опсин. Затем транс-ретиналь под действием энергии АТФ, которую приносят белки-переносчики, превращается в ретиналь, который соединяется с опсином.
Так восстанавливается родопсин. При наследственной мутации гена образуется неполноценный белок-переносчик. В результате нарушается восстановление родопсина и скапливается транс-ретиналь.
Он превращается в липофусцин и оказывает прямое токсическое действие на клетки-колбочки.
Виды заболевания зависят от распространенности зоны поражения желтого пятна. В офтальмологии различают следующие формы болезни Штаргардта: центральную, перицентральную, центропериферическую (смешанную). При центральной форме поражаются клетки в центре желтого пятна.
Это выражается в выпадении центрального зрения. У больного появляется центральная скотома (от гр. «скотос» — темнота). Выпадает из поля зрения центральная зона. Больной видит изображение с темным пятном в точке фиксации взгляда.
Перицентральная форма характеризуется появлением скотомы в стороне от точки фиксации. Человек способен фокусировать взгляд, но отмечает выпадения в одной из сторон от центра поля зрения в виде полумесяца. Со временем скотома приобретает вид темного кольца.
Центропериферическая форма начинается с центра и стремительно распространяется к периферии. Темное пятно разрастается и полностью перекрывает поле зрения.
Заболевание начинается в детском возрасте – это один из главных признаков для дифференциальной диагностики. С помощью офтальмоскопии обнаруживается широкое кольцо пониженной пигментации, которое окружает темный центр. Вокруг бледного кольца отмечается следующее кольцо гиперпигментированных клеток. Картина напоминает «бычий глаз» или «кованую бронзу». Фовеолярный рефлекс отрицательный. Макулярное возвышение не определяется. При осмотре желтого пятна отмечаются желтовато-белые пятна разной величины и конфигурации. Со временем границы включений размываются, пятна приобретают серый оттенок либо полностью исчезают. Во время проведения периметрии при болезни Штангардта отмечаются положительные или отрицательные (пациент их не ощущает) центральные скотомы. При центральной форме заболевания развивается красно-зеленая дейтеранопия. Для периферической формы не характерно нарушение цветового восприятия. Пространственная контрастная чувствительность изменяется по всему диапазону: отсутствует в области высоких частот (в центральном участке до 6-10 градусов) и снижается в области средних частот. В начальной стадии заболевания отмечается снижение показателей макулярной электрографии при центральной форме дистрофии. При дальнейшем прогрессировании электрические потенциалы не регистрируются. При расположении дистрофии по средней периферической зоне в начальной стадии отмечается нормальная электрография и электроокулография. Затем значения колбочковых и палочковых компонентов элетроретинографии снижаются до субнормальрных. Заболевание протекает бессимптомно – без нарушения остроты зрения и восприятия цвета. Границы поля зрения находятся в пределах нормы. Незначительно снижена темновая адаптация. С помощью флуоресцентной ангиографии на фоне «бычьего глаза» не обнаруживаются зоны гипофлуоресценции, просматриваются капилляры, «молчащая» или «темная» сосудистая оболочка. В зонах атрофии заметны гиперфлуоресцирующие участки клеток пигментного эпителия сетчатки. Гистологическое исследование в центральной зоне глазного дна определяет повышенное количество пигмента – липофусцина. Отмечается комбинация гипертрофированных и атрофированных клеток пигментного эпителия.
Молекулярно-генетический анализ позволяет заметить мутацию гена до начала проявлений болезни. Чтобы обнаружить замену нуклеотидов, проводится ПЦР в режиме реального времени при использовании нескольких ДНК-зондов – «молекулярных маяков».
Дифференциальная диагностика болезни Штаргардта осуществляется с приобретенными лекарственными дистрофиями, пятнами сетчатки Кандори, семейными друзами, ювенильным ретиношизисом, доминантной прогрессирующей фовеальной, колбочковой, колбочно-палочковой и палочко-колбочковой дистрофией.
Этиологического лечения нет. В качестве общего вспомогательного лечения применяются парабульбарные инъекций таурина и антиоксидантов, введение сосудорасширяющих средств (пентоксифиллин, никотиновая кислота), стероидных препаратов. Проводится витаминотерапия для укрепления сосудов и улучшения кровоснабжения (вит. Группы В, А, С, Е).
Показаны физиотерапевтические методы лечения: лекарственный электрофорез, ультразвук, лазерстимуляция сетчатки. Применяется методика реваскуляризации сетчатки путем трансплантации в зону желтого пятна пучка мышечных волокон.
Разрабатывается патогенетическая регенерационная офтальмологическая технология аутологичной тканевой терапии с помощью стволовых клеток жировой ткани пациента.
Болезнь Штаргардта начинается в раннем возрасте и быстро приводит к инвалидности по зрению. В редких случаях, при доминантном типе наследования, зрение падает медленно. Пациентам рекомендуется наблюдение офтальмолога, прием витаминных комплексов и ношение солнцезащитных очков.
42a96bb5c8a2acfb07fc866444b97bf1 Модератор контента: Васин А.С.
Болезнь Штаргардта
Болезнь Штаргардта — это наиболее общая форма наследственной подростковой макулярной дегенерации. Прогрессирующая потеря зрения, характерная для болезни Штаргардта, вызывается постепенной гибелью фоторецепторных клеток в центральной части сетчатки, которая называется макула.
Сетчатка — это тонкая светочувствительная ткань, расположенная на задней стенке глаза. Клетки фоторецепторов на сетчатке обеспечивают наше зрение, транслируя информацию, полученную в поле нашего зрения, в мозг. Макула отвечает за резкость центрального зрения, т.е., например, за такие задачи, как чтение, просмотр телевидения или распознавание лиц.
Ухудшение центрального зрения — это отличительный признак болезни Штаргардта. Периферическое зрение, как правило, при этой болезни сохраняется. Болезнь также затрагивает область глаза, которая находится под макулой и называется пигментным эпителием сетчатки.
Болезнь Штаргардта обычно развивается в детстве и юности.
Симптомы болезни Штаргардта
Симптом, который обычно заставляет большинство людей идти на прием к врачу, это изменение центрального зрения. А врач, который осматривает сетчатку пациента с болезнью Штаргардта, видит характерные желтоватые пятна на макуле и под ней. При этом пятна могут распространяться наружу кольцеобазным образом.
В пятнах происходит накопление липофусцина, побочного продукта нормальной активности клеток. При болезни Штаргардта это накопление идет очень интенсивно, и липофусцин аккумулируется анормальным образом.
Симптомы при этом заболевании также включают в себя волнистое видение, слепые пятна, размытость, нарушение цветового зрения и трудности с ориентацией при тусклом освещении.
Насколько быстро портится зрение?
Развитие симптомов болезни Штаргардта меняется со временем. Острота зрения (способность различать детали и резкость) может поначалу снижаться медленно, затем это ухудшение начинает ускоряться, а затем выравниваться на определенном уровне.
Исследование 95 пациентов с этим заболеванием показал, что, когда острота зрения снижается до уровня 20/40, часто начинается быстрое ухудшение зрения до уровня 20/200. (Нормальное зрение — это 20/20. Человек со зрением 20/40 видит на расстоянии 20 метров, в то время как человек с нормальным зрением видит на расстоянии 40 метров).
К 50-летнему возрасту острота зрения почти 50% из исследуемых пациентов составляла 20/200 или даже меньше.
В конечном итоге острота зрения почти всех людей с болезнью Штаргардта снижается на уровень от 20/200 до 20/400. Такая потеря зрения не корректируется очками, контактными линзами или рефракционной хирургией.
Является ли болезнь Штаргардта наследственной?
В 1997 году исследователи обнаружили ген болезни Штаргадта — ABCA4, который обычно вызывает образование белка, который необходим для жизнедеятельности клеток, определяющих наше зрение. Накопление липофусцина, видимо, связано с мутацией этого гена, что приводит в итоге к образованию неблагополучного белка.
Для того, чтобы понять, как происходит наследование этого заболевания, очень полезно проконсультироваться у специалиста по генетике, особенно при планировании семьи или выборе своей работы.
Лечение болезни Штаргардта
В настоящее время не существует действенного лечения этого заболевания, но сегодня ведется ряд перспективных исследований в этой области, связанных с генетикой, применением стволовых клеток и разработкой медикаментозной терапии.
Людям, которые страдают от этой болезни или находятся в зоне риска заболевания, рекомендуется на улице носить очки, блокирующие ультрафиолетовое излучение. Для людей, у которых зрение уже серьезно деградировало, существуют различные средства, предназначенные для слабовидящих.
Генная терапия
В 2008 году была опубликована информация о том, что генная терапия привела к измеряемым улучшениям зрения нескольких молодых людей, страдающих врожденным амаврозом Лебера, наследственным заболеванием, связанным с дегенерацией сетчатки глаз. Эти результаты, полученные во все еще продолжающихся клинических исследованиях (Phase I), заставили ученых попытаться найти аналогичный метод лечения и других наследственных заболеваний сетчатки, таких как болезнь Штаргардта.
Как и в случае болезни Штаргардта, амавроз Лебера возникает из-за мутаций генов, связанных с образованием белка, который необходим для жизнедеятельности сетчатки.
Во время эксперимента ученые внедрили здоровую версию такого гена в вирус (аденоассоциированный вирус*, ААВ), который выполняет функцию доставки гена в сетчатку. Этот вирус считается наиболее подходящим инструментом для внедрения относительно маленьких генов в целевой орган.
Кроме того, считается, что такой метод эффективен и безопасен для человека, поэтому он часто применяется при генной терапии.
Кроме ААВ для этой же цели может использоваться и лентивирус** — как показали эксперименты этот вирус может использоваться в качестве вектора (доставщика) полнофункциональных генов ABCA4 в фоторецепторы глаз мышей с болезнью Штаргардта.
Опыты по проверке концепции подобного лечения показали, что лечение мышей с болезнь Штаргардта с помощью лентивируса, содержащего полнофункциональные человеческие гены ABCA4, приводит к снижению накопления липофусцина в их сетчатке.
В настоящее время ведется тестирование клинической версии этого вирусного вектора на других животных, включая приматов.
Недавно компанией Oxford BioMedica была разработана запатентованная система LentiVector, которая использует лентивирусный вектор для доставки функциональных генов в целевые ткани.
Эта технология считается обещающей для лечения наследственных заболеваний глаз, таких как болезнь Штаргардта, палочко-колбочковая дистрофия, синдром Ашера (Ушера) и пигментный ретинит.
В 2011 году компания Oxford BioMedica начала клинические испытания (Phase I) для проверки терапии геном ABCA4 в качестве лечения болезни Штаргардта.
Сопутствующие заболевания
Болезнь Штаргардта иногда еще называют макулярной дистрофией Штаргардта или жёлтопятнистой абиотрофией сетчатки. Кроме рецессивной формы болезни Штаргардта существуют и другие, более редкие формы, которые наследуются как доминантный признак, а не рецессивный.
Фармацевтические и биотехнологические компании, разрабатывающие лечение болезни Штаргардта
Ниже приведены сведения о некоторых компаниях, которые в настоящее время разрабатывают новые методы лечения болезни Штаргардта.
Sanofi (http://en.sanofi.com/index.aspx)
Компания Sanofi разрабатывает генную терапию для лечения болезни Штаргардта, основанную на исследованиях доктора Алликмета, который использовал лентивирус для доставки нормально функционирующих генов ABCA4 в фоторецепторы сетчатки мыши с болезнью Штаргардта. В клинических исследованиях с участием людей (Phase I/II), начатых в 2011 году, проводилась оценка метода Stargen, основанная на проверке эффективности такой технологии. Эти эксперименты сейчас ведутся во Франции и США.
Acucela ( http://www.acucela.com/)
Эта биотехнологическая компания разрабатывает несколько препаратов для лечения болезней сетчатки, таких как возрастная макулярная дистрофия (ВМД), сухие глаза, диабетическая ретинопатия, ретинопатия недоношенных и болезнь Штаргардта. Модуляторы визуального цикла компании Acucela снижают активность работы палочек фоторецепторов, т.е.
«замедляют их», и снижают метаболическую нагрузку на сетчатку. Снижение скорости визуального цикла позволяет защитить сетчатку от светового повреждения и снижает накопление токсичных для сетчатки побочных продуктов, включая A2E (продукт преобразования витамина А), образующихся при болезни Штаргардта и сухой макулярной дистрофии.
Компания недавно завершила испытания (Phase III) нового лекарственного препарата эмиксустата как средства лечения сухой ВМД. К сожалению, этот препарат не смог снизить рост поражения у 500 пациентов с географической атрофией, одной из форм сухой ВМД.
Но поскольку этот препарат показал высокую эффективность при лечении болезни Штаргардта у мышей, компания начала исследования (Phase II) на пациентах с болезнью Штаргардта.
Astellas Pharma (https://www.astellas.us/ )
Компания работает как глобальный хаб (центр обмена) для исследований в сфере регенеративной медицины и клеточной терапии в офтальмологии и других терапевтических областях, в которых нет доступного лечения. В настоящее время Astellas завершила исследования метода трансплантации пигментного эпителия сетчатки и анонсировала проведения третьей фазы (Phase III) испытаний.
Alkeus (http://alkeus.com/)
Компания разработала форму витамина А, которая при взаимодействии со светом не образует токсичные метаболиты витамина А и A2E. Это вещество, ALK-001, представляет собой оральный препарат с хорошо понятным механизмом действия. Оно разработано специально для лечения болезни Штаргардта за счет предотвращения образования токсичных побочных продуктов витамина А.
Vision Medicines (http://visionmedicines.com/index.html)
Компания разрабатывает терапию малыми молекулами для лечения болезни Штаргардта. Vision Medicines открыла уникальное химическое вещество VM200, которое изолирует альдегидные токсины, такие как A2E. Компания планирует в ближайшем будущем проведение клинических исследований Phase I и Phase II.
* Аденоассоциированный вирус — малый вирус, инфицирующий клетки человека и некоторых других приматов. Он не вызывает заболевания у человека и, соответственно, вызывает слабый иммунный ответ.
Аденоассоциированный вирус может инфицировать делящиеся и неделящиеся клетки и может встраивать свой геном в геном хозяина.
** Лентивирусы — род вирусов из семейства ретровирусов с длительным инкубационным периодом. Они способны доставлять значительное количество генетического материала в клетку хозяина и обладают уникальной среди ретровирусов способностью реплицироваться в неделящихся клетках.
Болезнь Штаргардта — макулярная дистрофия сетчатки глаза — причины и лечение в Москве
Болезнь Штаргардта является наследственной патологией сетчатки глаза, сопровождающейся дегенеративными изменениями в ее центральной (макулярной) зоне, что влечет за собой утерю центрального зрения. Как правило, заболевание проявляет себя еще в детском или юношеском возрасте центральными скотомами и нарушением цветовосприятия.
При прогрессировании болезни Штаргардта, исходом процесса становится полная слепота. В диагностике патологии, применяют офтальмоскопию, флуоресцентную ангиографию и ЭФИ сетчатки. В качестве лечения, назначается инъекционная терапия препаратами витаминов, ангиопротекторов, антиоксидантов, а также физиотерапия.
Кроме того, проводятся реваскуляризирующие операции и применяется, находящаяся в разработке, методика аутологичной тканевой терапии.
Рис.1 Центральная (макулярная) зона сетчатки, которая поражается при болезни
О патологии
Болезнь Штаргардта носит и другое официалное название – ювенильная макулярная дегенерация. Именно оно наиболее полно отражает суть заболевания, которое начинается в раннем (ювенильном) возрасте.
Патология характеризуется поражением области макулы сетчатки – рецепторного аппарата анализатора зрения. Второе свое название болезнь получила по имени, описавшего ее в начале ХХ века, немецкого ученого Карла Штаргардта.
Патология описывалась, как врожденное поражение сетчатки в макулярной области, которое было характерно для представителей одного рода. Офтальмоскопические признаки заболевания полиморфны и типичны, это: атрофия хориоидеи, «битая (кованая) бронза», «бычий глаз».
Патогенетически, заболевание обозначается, как «желтопятнистая абиотрофия сетчатки», что отражает визуализируемые изменения на глазном дне.
Болезнь вызывает мутация гена АВСR с нарушением синтеза белка, отвечающего за транспорт энергии клеткам-фоторецепторам. Это было выяснено учеными-генетиками в 1997 году. Тогда же удалось доказать, что патология переносчика АТФ становится причиной гибели фоторецепторов сетчатой оболочки.
Наследственно обусловленная макулярной дегенерация – заболевание довольно частое, ее различные виды встречаются практически в половине случаев патологии глаз. Болезнь Штаргардта, при этом, составляет примерно 7% всех случаев. Частота нозологической формы болезни, характеризующейся прогрессирующим течением, составляет 1:10000 в популяции.
Патология имеет двусторонний характер течения, дебютирует в молодом возрасте (до 21 года) и очень часто становится причиной полной потери зрения. Социальная значимость болезни Штаргардта весьма велика, так как она приводит к инвалидности людей молодого трудоспособного возраста.
Причины возникновения
Наследование патологии происходит вне зависимости от половой принадлежности детей и родителей. Преимущественно она передается аутосомно-рецессивным путем, то есть поражает потомков родителей-носителей заболевания, однако не в 100% случаев. Последние исследования врачей-генетиков выявили, что патология гена способна передаваться также и по доминантному пути.
В случае доминантного пути передачи болезни, она протекает легче и к инвалидности приводит довольно редко. Большинство клеток- рецепторов в макуле (не верхушке желтого пятна) остаются функциональными, поэтому патология имеет минимум проявлений. Люди сохраняют работоспособность, острота зрения позволяет даже водить автотранспорт.
Главная причина дегенерации макулярных клеток — дефицит энергии.
Из-за дефекта гена, происходит синтез неполноценного белка, участвующего в транспорте молекул АТФ через мембрану клеток макулы – центра сетчатой оболочки, где и фокусируется цветное, графическое изображение. Желтое пятно не имеет кровеносных сосудов.
В питании клеток-колбочек принимают участие белки-переносчики АТФ из прилегающей сосудистой оболочки (хориоидеи). Именно эти белки транспортируют через мембрану молекулы АТФ внутрь клеток-фоторецепторов.
Родопсин фоторецепторов в нормальных условиях поглощает фотоны света, с превращением в опсин и транс-ретиналь. Затем, под действием энергии АТФ, приносимой белками-переносчиками, транс-ретиналь превращается в ретиналь и соединяется с опсином. Это процесс восстановления родопсина.
Наследственная мутация гена становится причиной синтеза неполноценного белка-переносчика. В итоге восстановление родопсина нарушается, происходит скопление транс-ретиналя. Он трансформируется в липофусцин, который и оказывает токсическое воздействие напрямую на клетки-колбочки.
Типы и виды болезни Штаргардта
Видовая изменчивость патологии объясняется распространенностью зоны поражения макулярной области. Специалисты классифицируют болезнь Штаргардта по следующим формам:
- Центральная.
- Перицентральная.
- Центропериферическая (смешанная).
Центральная форма характеризуется поражением клеток в центре области макулы. Процесс сопровождается выпадением центрального зрения. Человек отмечает появление центральной скотомы (темного пятна перед глазом). Происходит выпадение центральной зоны из поля зрения и видимое изображение в точке фиксации взгляда получается с темным пятном.
Перицентральная форма сопровождается возникновением в стороне от точки фиксации скотомы. Способность фокусировать взгляд остается, но с одной из сторон от центра поля зрения отмечает его выпадение в форме полумесяца. С прогрессом заболевания, скотома принимает вид темного кольца.
Для центрально-периферической формы характерно стремительное ухудшение зрения от центра к периферии. Постепенно разрастаясь, темное пятно полностью закрывает поле зрения.
Рис.2 Важность посещения врача-офтальмолога: чем раньше выявлена болезнь, тем выше шанс сохранить зрение
Признаки заболевания
Начало заболевания приходится на возраст 6-7 лет, тогда же возникают первые его симптомы. Вне зависимости от типа наследования, все пациенты отмечают возникновение центральных скотом. Ели, течение заболевания благоприятное, скотомы относительные.
Те есть, человек способен четко видеть яркие предметы, но объекты, имеющие слабую окраску, различает хуже. Многие больные страдают нарушением цветовосприятия по типу красно-зеленой дисхромазии, когда человек воспринимает зеленый цвет, как красный.
Правда, в некоторых случаях пациенты изменения цветового восприятия могут не отмечать.
В начальной стадии болезни, границы периферического зрения не изменены, но при прогрессировании центрально скотомы, они сужаются, что ведет к слепоте.
Одновременно с выпадением центрального зрения снижается и его острота. На итоговой фазе болезни Штаргардта происходит атрофия зрительного нерва и человек теряет зрение полностью. Изменений прочих глазных сред, на всех стадиях, не наблюдается.
Диагностика
Начало заболевания характерно для детского возраста. Это и является одним из главных диагностических его признаков.
При выполнении офтальмоскопии, выявляется широкое кольцо локализованное на сетчатке с пониженной пигментацией. Оно окружает темный центр здоровой ткани. Вокруг бледного кольца имеется следующее кольцо клеток с гиперпигментацией.
Офтальмологи определяют такую картину, как «бычий глаз», «кованая бронза». Макулярное возвышение не определяется, нет фовеолярного рефлекса. При осмотре области макулы определяются бело-желтые пятна разной конфигурации и размера.
Границы включений имеют тенденцию размываться со временем, пятна становятся сероватыми либо исчезают полностью.
Проведение периметрии при болезни Штангардта выявляет отрицательные (неощутимые) и положительные центральные скотомы.
Определяется красно-зеленая дейтеранопия, если патологический процесс протекает в центральной форме, и отсутствие нарушения цветового восприятия в периферической форме.
Изменение пространственной контрастной чувствительности по всему диапазону: ее отсутствие в зоне высоких частот (в центральном участке до 6-10 градусов), снижается в зоне средних частот.
Показатели макулярной электрографии в начальной стадии заболевания при центральной форме дистрофии снижены. Электрические потенциалы при дальнейшем прогрессировании процесса, не регистрируются.
Если дистрофии расположена по средней периферической зоне, нормальная электрография регистрируется только в начальной стадии. Затем при электроретинографии, значения компонентов колбочек и палочек становятся субнормальными.
Болезнь протекает без симптомов: нарушения остроты зрения и цветовосприятия не наблюдается. В норме границы поля зрения. Темновая адаптация снижена незначительно.
Флуоресцентная ангиография на фоне «бычьего глаза» зоны гипофлуоресценции не обнаруживает, капилляры просматриваются, сосудистая оболочка — «молчащая» или «темная».
Гиперфлуоресцирующие области клеток пигментного эпителия заметны лишь в зонах атрофии сетчатки. При гистологическом исследовании центральной зоны глазного дна выявляется излишнее количество липофусцина.
Клетки пигментного эпителия гипертрофированы и атрофированы в комбинации.
Проведение молекулярно-генетического анализа выявляет мутацию гена, произошедшую до начала заболевания. Изменение нуклеотидов, обнаруживается в режиме реального времени при проведении ПЦР с применением нескольких «молекулярных маяков» — ДНК-зондов.
Болезнь Штаргардта следует дифференцировать с приобретенными дистрофиями на фоне приема лекарств, пятнами Кандори, ювенильным ретиношизисом, семейными друзами, а также с прогрессирующей доминантной фовеальной колбочковой, палочко-колбочковой и колбочко-палочковой дегенерацией.
Рис.3 Осмотр глазного дна (офтальмоскопия) — основной метод диагностики заболевания
Лечение и прогноз
Как такового лечения, направленного на устранение заболевания нет. В качестве общей терапии показано внутриглазное введение таурина и антиоксидантов, расширяющих сосуды средств (никотиновая кислота, пентоксифиллин), гормональных препаратов.
Также назначается витаминотерапия (вит. группы В, А, С, Е), направленная на укрепление сосудов, чтобы улучшить кровоснабжение и питание пораженной зоны сетчатки, ретинопротекторы (ретиналамин).
Целесообразно проведение физиотерапии: ультразвук, лекарственный электрофорез, лазерстимуляция.
В домашних условиях пациенты могут смомостоятельно применять вакуумный массаж — прибор АМВО-01, разработанный специалистом по заболеваниям сетчатки у детей д.м.н., профессором Сидоренко Евгением Ивановичем, который не только стабилизирует процесс, но и даёт повышение остроты зрения и расширение полей.
Из хирургических методик нами применяется реваскуляризация заднего отдела глаза — процедура по активизации обменных процессов и улучшению кровоснабжения центральной области сетчатки.
В стадии разработки находится метод реваскуляризации сетчатки посредством пересадки в макулярную зону пучка мышечных волокон. Кроме того, на этапе исследования находится технология патогенетической регенерационной аутологичной тканевой терапии с использованием стволовых клеток жировой ткани пациента.
Для болезни Штаргардта характерно начало в детском возрасте и быстрый прогресс до состояния инвалидизации пациента по зрению. Зрение ухудшается медленно только в очень редких случаях доминантного пути наследования заболевания. В качестве профилактики, рекомендуется прием витаминных комплексов, длительное наблюдение офтальмолога, применение солнцезащитных очков.
Пациенты с болезнью Штаргардта нуждаются в динамическом наблюдении врача-ретинолога. Специалисты нашей клиники – признанные лидеры лечения заболеваний сетчатки.
Применение инновационных технологий, новейшая аппаратура от лучших мировых производителей и индивидуальный подход к каждому пациенту, обеспечивают гарантированное получение максимально высоких результатов даже в самых сложных случаях.
Штаргардта болезнь
Болезнь Штаргардта 1 типа (Stargardt disease, STGD) и абиотрофия сетчатки типа Франческетти (фундус флавимакулятус (FFM) или желтопятнистое глазное дно) относятся к наследственным абиотрофиям сетчатки — гетерогенной группе наследственных заболеваний сетчатки глаза, обусловленных дегенеративными изменениями фоторецепторных клеток пигментного эпителия и приводящих к значительному снижению остроты зрения. Болезнь Штаргардта является одной из наиболее частых наследственных дистрофий макулярной области сетчатки.STGD, являющаяся классическим примером центральной пигментной дегенерации сетчатки, проявляется в детском и молодом возрасте (7-20 лет). Заболевание дебютирует снижением остроты центрального зрения, как правило, в возрасте 7-9 лет, затем медленно прогрессирует с присоединением грубых нарушений цветоощущения на все цвета. Изменения на глазном дне, хотя и полиморфны, характеризуются появлением в обоих глазах пигментированных круглых точек, участков депигментации и атрофии пигментного эпителия сетчатки, сочетающихся часто с беловато- желтоватыми пятнами в парамакулярной зоне. Изменения в виде желтовато-беловатых точек и полос с изменениями в макулярной области или без них A. Franceschetti обозначил термином «fundus flavimaculatus» (абиотрофия сетчатки типа Франческетти). В литературе термины «болезнь Штаргардта» и «фундус флавимакулятус» нередко объединяют, подчеркивая тем самым предполагаемое единство происхождения. Клиническими проявлениями STGD также являются снижение остроты зрения, потеря цветового зрения, фотофобия, парацентральная скотома и слабая адаптация к темноте. Гистологически заболевание характеризуется избыточным накоплением липофусцин-подобного вещества в пигментном эпителии сетчатки, главным образом в тех его участках, которые имеют в своем составе колбочковые фоторецепторы.STGD и FFM наследуются по аутосомно-рецессивному типу, когда ребенок получает по гену с мутацией от обоих родителей. Частота заболевания составляет 1 случай на 10.000 новорожденных.Одной из генетических причин, приводящей к наследственным абиотрофиям сетчатки, является повреждение гена ABCA4 (АВСR). ABCR является специфическим белком нейросенсорных клеток сетчатки, необходимым для их нормального функционирования и зрения. Ген ABCR располагается в хромосомном регионе 1р22.1-р21, состоит из 50 экзонов, кодирует 2273 аминокислоты и имеет протяженность ~ 150 т.н.п.
На сегодняшний день известно более 400 разных мутаций в гене ABCA4, приводящих к наследственным абиотрофиям сетчатки.
Мутации в гене CNGB3 могут приводить к развитию болезни Штаргардта 1 типа. Ген CNGB3 находится на длинном плече хромосомы 8 (8q21.3) и состоит из 18 экзонов. Этот ген кодирует бета-3-субъединицу G-белка.
G-белки экспрессируются во всех клетках организма и играют главную роль в передаче сигналов от множества рецепторов с поверхности клетки. Описано около 40 мутаций.
Мутации в гене CNGB3 также приводят к развитию ахроматопсии тип 3.
Болезнь Штаргардта 3 типа (Stargardt disease 3, STGD3) (OMIM 600110) имеет клинические проявления, сходные с болезнью Штаргардта 1 типа, но наследуется по аутосомно-доминантному типу, когда для проявления заболевания достаточно одной мутации. Болезнь Штаргардта 3 типа вызывается мутациями в гене ELOVL4
Клиника коррекции зрения профессора Трубилина
Возрастная макулярная дегенерация – основная причина слепоты у людей старше 60 лет. Заболевание характеризуется повреждением макулы, которая является наиболее чувствительной к свету областью сетчатки. В лечении используют хирургические подходы и лекарственные средства, позволяющие замедлить прогрессирование патологии.
Причины возникновения
Выявить конкретную причину развития возрастной макулярной дегенерации (ВМД) не удается. Заболевание развивается у людей в пожилом возрасте. Известно, что болезнь имеет генетическую предрасположенность и может носить семейный характер. Если в семье уже отмечались случаи заболевания у родственников первой линии, то вероятность развития болезни у наследников очень велика.
Основные факторы риска развития возрастной макулярной дегенерации:
- Возраст старше 60-65 лет, когда организм подвергается естественному старению и износу тканей.
- Европеоидная раса.
- Случаи макулярной дегенерации в семье. Вероятность развития патологии при наличии ВМД у одного из родителей – более 20%.
- Хронические заболевания сердечно-сосудистой системы: атеросклероз, гипертоническая болезнь и прочие патологии этого профиля.
- Табакокурение, так как никотин негативно влияет на сосуды в сетчатке, замедляет кровообращение в организме.
- Питание с высоким содержанием насыщенных жирных кислот и холестерина.
- Любой вариант катаракты в анамнезе пациента.
При наличии указанных факторов риска человеку рекомендуется регулярно посещать врача-офтальмолога для своевременного выявления макулярной дегенерации. Визит в клинику для стандартного осмотра обязателен с частотой не реже 1 раза в год.
Формы патологии
Возрастная макулярная дегенерация может протекать в двух вариантах: сухом и влажном. Основное отличие между ними – наличие при влажной форме экссудата и новообразованных сосудов. Вне зависимости от типа ВМД, болезнь развивается из-за образования в клетках сетчатки большого количества свободных форм кислорода. Они повреждают чувствительные к свету клетки, вызывая нарушения зрения.
Сухая форма болезни встречается у 85% больных. При осмотре у офтальмолога специалист отмечает образование в области макулы желтоватых пятен различного размера. Это участок атрофии, характеризующийся разрушением ретинальных клеток. В отсутствии лечения его размеры быстро прогрессируют.
Влажная форма макулярной дегенерации имеет худший прогноз для пациентов. Она возникает остро, характеризуется резким снижением остроты зрения. В сетчатке выявляют образование большого количества сосудов. Они имеют аномальное строение и приводят к формированию экссудата, который скапливается в области макулы, нарушая питание клеток.
Клинические проявления
Возрастная макулярная дегенерация характеризуется медленной, безболезненной и необратимой потерей зрения. Слепота у некоторых больных может наступить резко. Первые симптомы заболевания: снижение остроты зрения, трудности при чтении, шитье, особенно при недостаточном освещении.
Некоторые пациенты жалуются на искажение форм и размеров предметов. Реже страдает цветовосприятие. Клинические проявления возрастной макулярной дегенерации при поражении одного глаза выражены слабо. Как правило, люди обращаются к офтальмологу при двустороннем поражении сетчатки.
Ухудшение предметного зрения с выпадением его центрального поля – основной признак возрастной макулярной дегенерации.
Пациент отмечает появление пятен черного или серого цвета, а также нечеткость предметов, изменение их формы при попытке их рассмотреть.
В результате этого больной не может смотреть ТВ, управлять автомобилем, читать, писать и распознавать лица. При прогрессировании болезни ухудшается периферическое зрение.
Снижение центрального зрения приводит к искажению восприятия контрастности. Человек не отличает текстуру и незначительные изменения в предметах. Например, некоторые больные не видят ступеньки или переходы высоты на тротуарах. В результате этого возможны падения и травмы.
Диагностика возрастной макулярной дегенерации
Выявлением заболевания и его терапией занимается офтальмолог. Самолечение недопустимо, так как макулярная дегенерация имеет тенденцию к постоянному прогрессированию с развитием тяжелых осложнений, вплоть до полной слепоты.
Обследование начинают с беседы. Специалист собирает имеющиеся жалобы, их характер и время появления, а также расспрашивает больного об имеющихся факторах риска. Это позволяет заподозрить ВМД, а при необходимости назначить дополнительные методы исследования:
- Фундоскопия (осмотр глазного дна). Офтальмолог выявляет участки атрофии желтоватого цвета в области макулы. Если на сетчатке имеется большое количество извитых сосудов, то это свидетельствует о влажной форме болезни.
- Тест Амслера ― позволяет выявить нарушения восприятия предметов. Исследование проводят с помощью одноименной сетки. Если у пациента имеется макулярная дегенерация, то линии приобретают изломанный и волнистый характер. В центре поля зрения появляются темные пятна, затрудняющие обзор, нарушающие видение.
- Флуоресцентная ангиография ― проводят при подозрениях на влажную форму ВМД, которая проявляется образованием аномальных сосудов в области макулы. Повышенная флюоресценция сетчатки подтверждает диагноз.
- Современный метод диагностики – оптическая когерентная томография, в результате которой получают трехмерное изображение сетчатки. При ее дегенерации, в области макулы появляется участок атрофии.
В процессе лечения проводятся повторные исследования. Они необходимы для выявления осложнений патологии и перехода сухой формы ВМД во влажную, которая имеет худший прогноз. Динамическое обследование проводят по 2-3 раза в год.
Лечение возрастной макулярной дегенерации в Москве
Полное выздоровление невозможно. При правильном подборе лечения прогрессирование болезни останавливается, а у больного можно добиться улучшения зрения. Терапия включает в себя лекарственные препараты, диету и хирургические вмешательства.
Хирургический метод лечения применяется только в том случае, если иные методы коррекции не дали прогнозируемого результата. Он позволяет устранить поврежденные участки сетчатки.
Операции проводят при наличии показаний: геморрагических осложнений в виде кровоизлияний, быстром прогрессировании патологии. Больным осуществляют витрэктомию, во время которой удаляют стекловидное тело, иссекают мембрану под сетчаткой.
При выраженных морфологических изменениях возможности оперативного вмешательства ограничены.
При влажной форме болезни высокой эффективностью обладают ингибиторы ангиогенеза. Они блокируют образование новых сосудов. Препараты вводятся интравитреально, то есть в стекловидное тело. Основные лекарственные средства: Пегаптаниб, Ранибизумаб, Афлиберцепт и прочие. Указанные средства позволяют улучшить зрение и предупредить последствия влажной формы возрастной макулярной дегенерации.
Высокой эффективностью при влажной форме обладает лазерная коагуляция. Воздействие лазером позволяет нарушить кровоток в аномальных сосудах и предупредить образование экссудата. Недостаток метода – повреждающее действие лазерной энергии на фоторецепторы в области макулы. Это ограничивает его применение в клинической практике.
Фотодинамическая терапия основана на разрушении кровеносных сосудов после введения препарата Визудина. Он повышает чувствительность клеток сетчатки к свету с определенной длиной волны. Это позволяет закрыть просвет кровеносных сосудов и предупредить прогрессирование влажной формы ВМД.
Прогноз для пациента
Возрастная макулярная дегенерация относится к неизлечимым болезням. Полное выздоровление невозможно, так как фоторецепторы на сетчатке не восстанавливаются. Основная задача терапии – предупредить прогрессирование нарушений. Без терапии болезнь прогрессирует, и может стать причиной полной слепоты.
Потеря центрального зрения и нарушения восприятия предметов – основные признаки возрастной макулярной дегенерации. При обнаружении первых симптомов патологии обратитесь в Клинику доктора Трубилина. Здесь вам подберут лучшие варианты терапии, чтобы остановить болезнь и нормализовать здоровье зрительного органа.


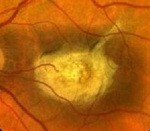 Болезнь Штаргардта
Болезнь Штаргардта 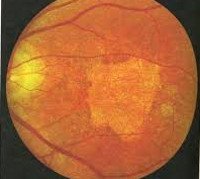 Болезнь Штаргардта Наследование не зависит от половой принадлежности пациента и родителей. Патология передается преимущественно по аутосомно-рецессивному типу, то есть наследование патологии не связано с полом (аутосомное – связано с неполовыми хромосомами) и не всегда передается будущему поколению (рецессивный путь наследования). По последним данным врачей-генетиков, патология гена может передаваться и по доминантному типу. При доминантном типе наследования дефектов гена – контролера синтеза белка-транспортера АТФ – заболевание протекает легче и нечасто приводит к инвалидности. Большинство рецепторных клеток макулы (верхушки) желтого пятна глазного дна функционируют. У пациентов с доминантным типом наследования болезнь протекает с минимумом проявлений. Больные сохраняют работоспособность и могут даже водить автотранспорт. Основная причина дегенерации клеток макулы заключается в том, что они страдают от дефицита энергии. Дефект гена приводит к синтезу неполноценного белка, транспортирующего молекулы АТФ через мембрану клеток желтого пятна – центра сетчатки глаза, в котором фокусируется графическое и цветное изображение. В области желтого пятна нет кровеносных сосудов. Питание клеток-колбочек осуществляется за счет белков-переносчиков АТФ из близлежащей сосудистой оболочки (хориоидеи). Белки переносят через мембрану внутрь клеток-колбочек молекулы АТФ.
Болезнь Штаргардта Наследование не зависит от половой принадлежности пациента и родителей. Патология передается преимущественно по аутосомно-рецессивному типу, то есть наследование патологии не связано с полом (аутосомное – связано с неполовыми хромосомами) и не всегда передается будущему поколению (рецессивный путь наследования). По последним данным врачей-генетиков, патология гена может передаваться и по доминантному типу. При доминантном типе наследования дефектов гена – контролера синтеза белка-транспортера АТФ – заболевание протекает легче и нечасто приводит к инвалидности. Большинство рецепторных клеток макулы (верхушки) желтого пятна глазного дна функционируют. У пациентов с доминантным типом наследования болезнь протекает с минимумом проявлений. Больные сохраняют работоспособность и могут даже водить автотранспорт. Основная причина дегенерации клеток макулы заключается в том, что они страдают от дефицита энергии. Дефект гена приводит к синтезу неполноценного белка, транспортирующего молекулы АТФ через мембрану клеток желтого пятна – центра сетчатки глаза, в котором фокусируется графическое и цветное изображение. В области желтого пятна нет кровеносных сосудов. Питание клеток-колбочек осуществляется за счет белков-переносчиков АТФ из близлежащей сосудистой оболочки (хориоидеи). Белки переносят через мембрану внутрь клеток-колбочек молекулы АТФ.